ZERVIXKARZINOM
Das Zervixkarzinom ist ein bösartiger Tumor im unteren Teil der Gebärmutter – dem Gebärmutterhals. Das Zervixkarzinom ist mit einer Inzidenz von jährlich weltweit circa 500.000 Betroffenen die vierthäufigste Krebserkrankung der Frau. Ursache ist häufig eine Infektion mit bestimmten Typen des humanen Papillomvirus (z. B. HPV Typ 16 und 18). Besteht solch eine HPV-Infektion über längere Zeit, können sich Krebsvorstufen bilden. Ebenfalls können sich bei persistierender HPV-Infektion zervikale intraepitheliale Neoplasien (CIN) bzw. "Squamous Intraepithelial Lesions" (SIL) bilden. Sie stellen eine Präkanzerose dar. Werden diese nicht behandelt, so kann sich aus ihnen Gebärmutterhalskrebs entwickeln. Dabei ist das Virus nicht alleiniger Verursacher, aber Krankheits-Grundlage für verschiedene Co-Risikofaktoren. HPV wird durch Sexualkontakte übertragen. In frühen Stadien ist Gebärmutterhalskrebs meist gut heilbar. In Deutschland hat jede Frau ab 20 Jahren Anspruch auf eine kostenlose Gebärmutterhalskrebs-Früherkennung. Ein wichtiger Teil der Untersuchung ist ein Zellabstrich vom Gebärmutterhals, der sogenannte Pap-Abstrich. Dabei streicht die Frauenärztin oder der Frauenarzt Zellen vom Gebärmutterhals ab und schickt sie in ein Labor. Dort werden die Zellen unter dem Mikroskop untersucht. Neu seit 2020: Frauen ab 35 Jahren bietet das Früherkennungsprogramm statt des jährlichen Pap-Abstrichs nun alle 3 Jahre eine Kombination aus HPV-Test und Pap-Abstrich an. Durch diese Möglichkeit, Dysplasien frühzeitig nachzuweisen und zu behandeln ist das Zervixkarzinom nicht mehr der häufigste gynäkologische Tumor.
Im frühen Stadium macht das Zervixkarzinom, bzw. seine Vorstadien keine Symptome. Eine lymphogene Metastasierung tritt jedoch früh auf, v.a. in die Parametrien und Beckenlymphknoten. Relativ spät tritt hingegen eine hämatogene Metastasierung auf, dann erfolgt vornehmlich der Befall von Leber, Lunge und Skelett.
Ab einer gewissen Größe und Ausdehnung des Tumors treten Symptome wie Zwischenblutungen, Fluor genitalis, Kontaktblutung und Schmerzen bei der Kohabitation auf, bei Fernmetastasen entsprechende Beschwerden je nach Lokalisation der Metastasen.
Die Behandlung des fortgeschrittenen Zervixkarzinoms ist ab diesem Zeitpunkt nach wie vor eine Herausforderung.
Die aktuelle Standardversorgung – Radiochemotherapie mit anschließender Brachytherapie – geht mit erheblicher Toxizität einher. Die Raten des vollständigen pathologischen Ansprechens bei
Induktionschemotherapie liegen zwischen 11 und 20 %. Bezüglich des Überlebens gibt es keinen Unterschied zwischen Chemotherapie, Operation oder Strahlentherapie allein, was auf die Resistenz
der Tumorzellen gegen Chemotherapeutika und deren niedrigen Spitzenkonzentrationen innerhalb eines Tumors zurückzuführen ist.
Bei einer Regionalen Chemotherapie in Form der Isolierten Hypoxischen Perfusion (HPP) sind diese Einschränkungen nicht gegeben.

Tumoransprechen und Lebensqualität nach der isolierten hypoxischen Beckenperfusion bei fortgeschrittenem Zervixkarzinom Grad G3: Eine Fallserie
Folgend berichten wir über eine im Oktober 2020 im International Journal of Surgery Case Reports (IJSCR 77 2020; 816-821) veröffentlichte Fallserie über drei Patientinnen mit fortgeschrittenem Zervixkarzinom, histologisch Grad G3, die eine Standardbehandlung ablehnten und sich für eine isolierte hypoxische Beckenperfusion (HPP, hypoxic pelvic perfusion) entschieden.
Zusammenfassung
Einführung: Vorgestellt wird eine Fallserie aus drei Patientinnen mit fortgeschrittenem Zervixkarzinom, die entweder die Standardtherapie mit systemischer Chemotherapie oder Radiochemotherapie ablehnten oder diese keinen Nutzen hatte.
Methodik: Wir behandelten die Patientinnen mittels der isolierten hypoxischen Beckenperfusion (HPP, hypoxic pelvic perfusion).
Ergebnisse: Zwei Patientinnen zeigten ein vollständiges klinisch-pathologisches Ansprechen, bei einer Patientin war eine chirurgische Exzision einer nekrotischen Resttumormasse ohne vitale Tumorzellen notwendig. Langfristig zeigten sich keine systemischen oder lokalen Nebenwirkungen. Alle Patientinnen sind bis zu 15 Jahre nach Abschluss der Behandlung weiterhin tumorfrei.
Schlussfolgerung: Die regionale Chemotherapie in Form der isolierten hypoxischen Beckenperfusion stellt eine wirksame Therapieoption zur Behandlung des fortgeschrittenen Zervixkarzinoms dar, die eine schnelle und anhaltende Remission bei geringen Nebenwirkungen erzielt.
Methodik
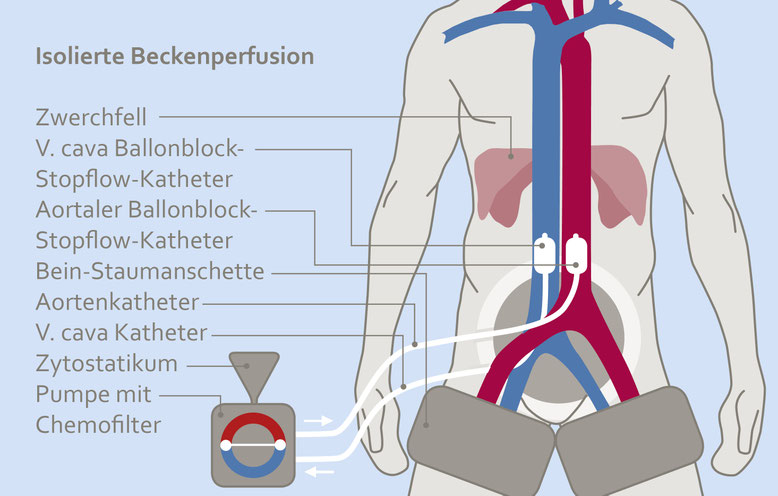
Technik der isolierten hypoxischen Beckenperfusion
Die Arteria und Vena femoralis werden mittels einer kleinen Inzision unter Vollnarkose freigelegt. Distal zur Inzision werden bilaterale pneumatische Manschetten eingesetzt. Wir kanülieren beide Gefäße mit dreilumigen Stop-Flow-Ballonkathetern und verwenden einen Führungsdraht, um die Ballons unter Durchleuchtung auf gleicher Höhe über die Bifurkation der Aorta und der Vena cava inferior vorzuschieben.
Dann werden die Ballons entblockt, und die Patienten erhalten für 3–5 Minuten 100 % Sauerstoff. Danach werden Cisplatin, Adriamycin und Mitomycin schnell über den arteriellen Zugang infundiert und die Ballons wieder geblockt, um einen isolierten Kreislauf für 15 Minuten herzustellen. Anschließend werden die Ballons entleert und die Zytostatika über einen Zeitraum von 30 Minuten über die Perfusionskatheter mit 4 l des Filtrats wieder herausgefiltert, um die systemische Exposition zu verringern. Die Katheter werden entfernt und die Gefäße mittels fortlaufender Naht verschlossen.
Wir stellen hier retrospektive Einzelfälle vor, die in Langzeitintervallen mit der gleichen Methode der isolierten hypoxischen Beckenperfusion behandelt wurden.
Fall 1
Im ersten Fall handelt es sich um eine 48-jährige Patientin mit fortgeschrittenem Zervixkarzinom, UICC-Stadium IVA, mit präsakralen Lymphknotenmetastasen. Histologie: Plattenepithelkarzinom, Grad G3. Die explorative Laparotomie bestätigte eine rektale Invasion.
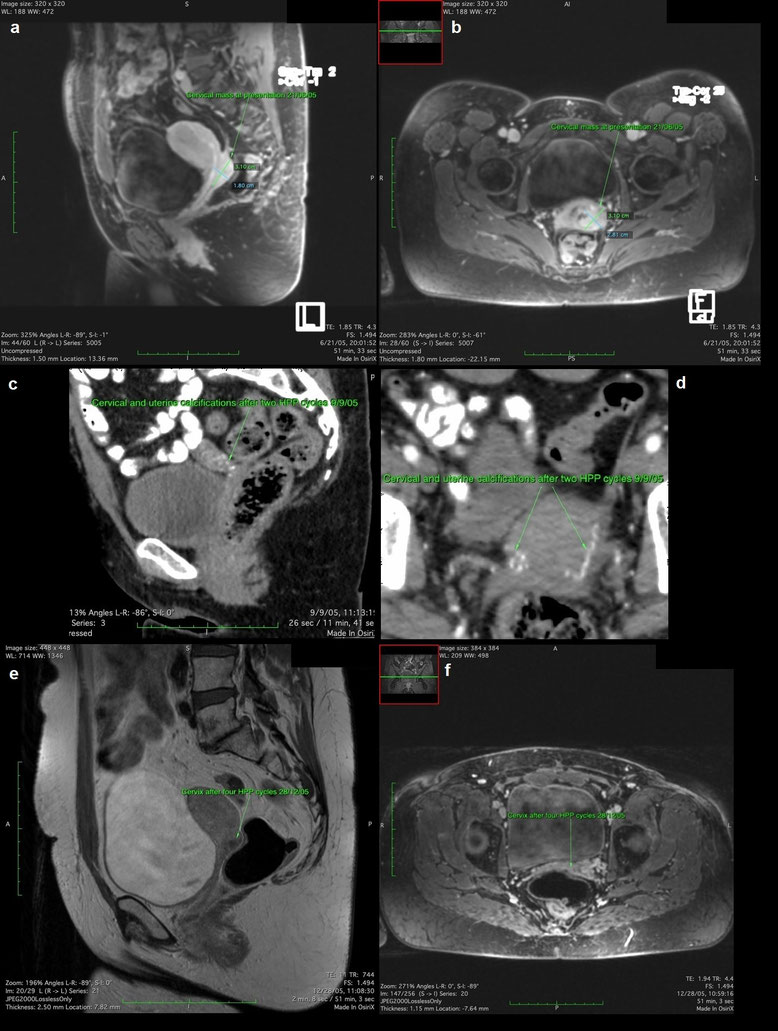
Die Patientin erhielt im Mai 2005 zwei Behandlungszyklen mit Carboplatin und Taxol. Ein MRT des Abdomens und des Beckens im Juni 2005 zeigte eine 3,1 x 1,8 x 2,8 cm große Raumforderung, die das dorsale Vaginalgewölbe, die rechte Plica rectouterina bis in das Rektum und präsakrale Weichteile links infiltrierte. Die Patientin lehnte eine Radiochemotherapie ab.
Die Patientin erhielt drei HPP-Zyklen mit 50 mg Cisplatin, 30 mg Adriamycin und 20 mg Mitomycin je Zyklus.
Ein CT des Abdomens und Beckens vom September 2005 nach zwei HPP-Zyklen zeigte ausgedehnte Verkalkungen in der Zervix und im Uterus. Nach zwei weiteren HPP-Zyklen zeigte ein MRT des Abdomens und des Beckens im Dezember 2005, eine nekrotische Resttumormasse im Gebärmutterhals.
Im Februar 2006 führten wir eine radikale Hysterektomie durch, die das vollständige pathologische Ansprechen bestätigte. Die Patientin erhielt einen adjuvanten HPP-Zyklus mit 50 mg Cisplatin, 30 mg Adriamycin und 30 mg Mitoxantron. Die Patientin wurde einmal jährlich mittels MRT kontrolliert. Diese ergaben keine Anzeichen eines Rezidivs. Die Patientin ist seit 15 Jahren tumorfrei bei sehr guter Lebensqualität.
Fall 2
Bei dem zweiten Fall handelt es sich um eine 46-jährige Patientin mit fortgeschrittenem Zervixkarzinom im UICC-Stadium IIIA mit Beteiligung von Parametrium und Vagina. Die Diagnose wurde gestellt nachdem sie mit Schmerzen im Beckenbereich bei ihrem Gynäkologen vorstellig geworden war.
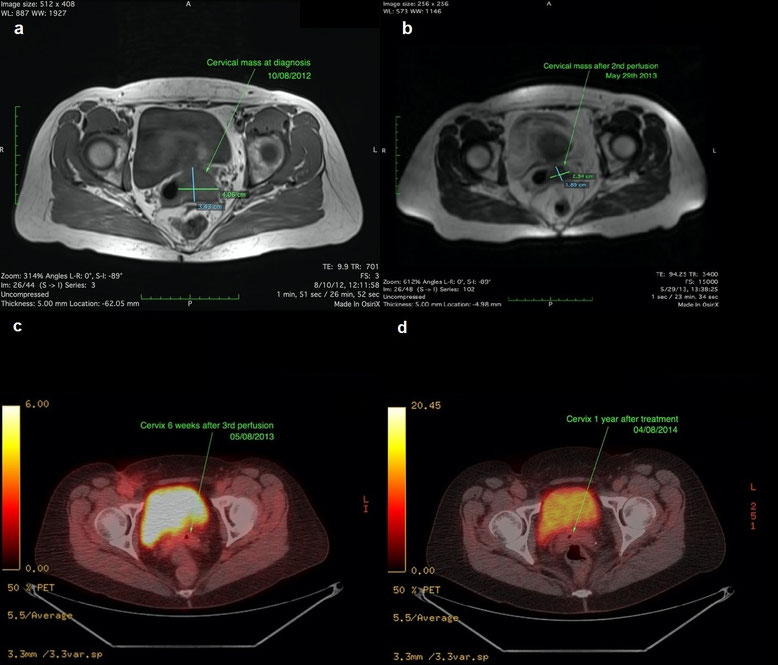
Ein MRT im August 2012 zeigte eine zervikale Raumforderung von 3,43 x 4,06 cm. Eine CT-Untersuchung des Abdomens und Beckens offenbarte im April 2013 eine zervikale Raumforderung mit einer Größe von 3,86 x 5,83 cm. Es lag kein Hinweis auf eine metastasierende Erkrankung vor. Der behandelnde gynäkologische Onkologe teilte der Patientin mit, dass sie an einer inoperablen Erkrankung leide. Die Patientin stellte sich kurze Zeit später in unserer Klinik vor.
Nach den ersten zwei HPP-Zyklen mit jeweils 50 mg Cisplatin, 30 mg Adriamycin und 15 mg Mitomycin ergab die gynäkologische Untersuchung einen verkürzten Gebärmutterhals mit Vernarbungen und ohne
Anzeichen eines zervikalen oder vaginalen Tumors. Die parametrische Untersuchung erbrachte tastbares Narbengewebe mit verbesserter Mobilität. Die Patientin war schmerzfrei.
Sie erhielt einen zusätzlichen HPP-Zyklus im Juni 2013. Ein MRT des Abdomens und Beckens zeigte im Mai 2013 nach zwei HPP-Zyklen eine zervikale Resttumormasse von 1,89 x 2,34 cm Größe.
Ein im August 2013 durchgeführtes FDG PET-CT zeigte eine unauffällige Zervix ohne metabolische Aktivität. Das im August 2014 zur Nachkontrolle durchgeführte FDG PET-CT zeigte keine Anzeichen
eines Rezidivs.
Die Patientin ist seit 7 Jahren tumorfrei.
Fall 3
Bei dem dritten Fall handelt es sich um eine 63-jährige Patientin mit Zervixkarzinom, UICC-Stadium III, Grad G3. Sie hatte im Dezember 2017 eine Kürettage und
Konisation, pathologisches Stadium pT1b1, cN0, cMx, L1, V1, R1. Sie lehnte eine leitlinienbasierte Therapie ab und begann stattdessen mit einer naturheilkundlichen Behandlung. Ein CT des Abdomens
und Beckens im November 2019 zeigte iliakale Lymphknotenmetastasen beidseitig und eine voluminöse Zervix mit tiefer Infiltration des Myometriums.
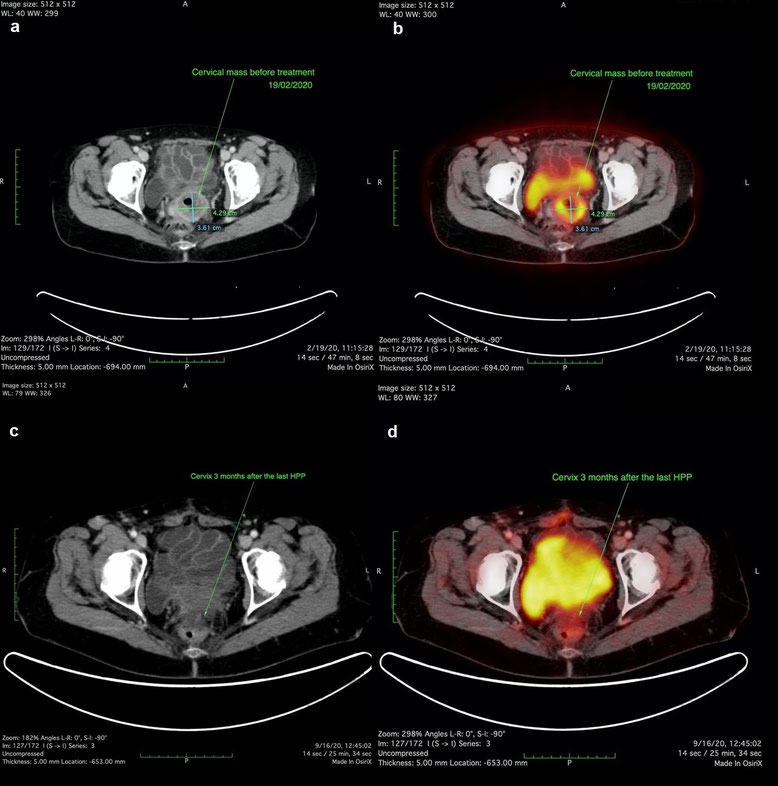
Die Patientin wurde im Februar 2020 mit wiederkehrenden vaginalen Blutungen in unserer Klinik vorstellig. Ein CT des Abdomens und Beckens und ein FDG PET-CT, welche im Februar 2020 durchgeführt wurden, bestätigten eine hoch metabolische zervikale Läsion von 3,61 x 4,29 cm Größe. Die Patientin entschied sich die regionale Chemotherapie mit HPP fortzusetzen.
Wir führten die HPP mit 50 mg Cisplatin, 30 mg Adriamycin und 15 mg Mitomycin jeweils im März und April 2020 durch. Die Vaginalblutungen stoppten zu Beginn des zweiten Zyklus. Das im Mai 2020 durchgeführte CT des Abdomens und Beckens zeigte eine 2,90 x 3,24 cm große verbliebene zervikale Läsion.
Die Patientin erhielt im Juni 2020 eine weitere isolierte Beckenperfusion. Über systemische Toxizität wurde nie berichtet.
Das im September 2020 durchgeführte FDG PET-CT zeigte keine auffällige Stoffwechselaktivität.
Diskussion
Die Radiochemotherapie, gefolgt von einer intrakavitären Brachytherapie, ist die Standardbehandlung des fortgeschrittenen Zervixkarzinoms. Das rezidivfreie Überleben (DFS, disease-free survival) liegt bei 85–90 %, geht jedoch aufgrund der Toxizität eines platinbasierten Therapieregimes und der verstümmelnden Wirkung der Strahlentherapie mit einer signifikanten Morbidität einher.
Zu den üblichen Nebenwirkungen gehören vaginale Trockenheit, Harnröhrenstrikturen, vesikovaginale und rektovaginale Fisteln, Lymphostase und Lymphozele. Keine der genannten Nebenwirkungen wurden bei unseren Patientinnen beobachtet.
Das rezidivfreie Überleben nach Cisplatin-basierter Radiochemotherapie und Radikaloperation ist dem der Induktionschemotherapie und anschließender Radikaloperation überlegen. Die intensitätsmodulierte Strahlentherapie reduzierte die Toxizität um fast 50 %, nach wie vor führt sie allerdings in etwa 30 % der Fälle zu schweren Nebenwirkungen.
Es wurden mehrere Versuche unternommen, um herauszufinden, ob eine Induktionschemotherapie ausreicht, um ein angemessenes Ansprechen zu erzielen und die Resektabilität sicherzustellen. Die Metaanalyse einer Radikaloperation mit oder ohne Induktionschemotherapie zeigte keinen Effekt der Induktionschemotherapie auf das rezidivfrei (DFS) oder progressionsfreie Überleben (PFS, progression-free survival). Mehrere kleinere Studien zeigten vergleichbare Ergebnisse zu intraarteriellen Infusionen von Chemotherapeutika.
Aus diesem Grund besteht weiterer Bedarf an alternativen Ansätzen, um ein optimales PFS, DFS und eine optimale Lebensqualität (QOL, quality of life) zu erreichen.
Wir konnten zeigen, dass die isolierte hypoxische Perfusion mit anschließender Chemofiltration eine höhere Penetration der Zytostatika in den Tumor ermöglicht, was nach drei oder vier Behandlungszyklen zu einem dauerhaften Ansprechen ohne signifikante systemische Toxizität führte. Die Verwendung von Immun-Checkpoint-Inhibitoren bei ausgewählten Patienten könnte das Ansprechen weiter verbessern.
Die vorgestellten Fälle zeigen hervorragende Ergebnisse bei fortgeschrittenen Zervixkarzinomen, was bei anderen Tumorarten die ebenfalls mittels intraarterieller Chemotherapie und isolierter hypoxischer Perfusion behandelt werden, häufig der Fall ist.
Schlussfolgerung
Wir konnten die Wirksamkeit der HPP bei der Erzielung einer vollständigen und dauerhaften klinischen und radiologischen Remission ohne erkennbare Anzeichen systemischer Toxizität zeigen.
Es besteht sicherlich der Bedarf an einer prospektiven randomisierten Studie, in der die derzeitigen Standardtherapien und die isolierte hypoxische Perfusion verglichen werden.
Literatur
Kornelia Aigner, Rita Schlaf, Elmar Müller-Wühr, Karl R. Aigner (2022)
Metastatic Cervical Cancer - successive treatment of isolated locations
DOI: 10.1016/j.ejso.2021.12.292