IMMUNTHERAPIE
Das Immunsystem ist prinzipiell in der Lage maligne Tumorzellen zu erkennen und anzugreifen. Dazu muss einerseits sichergestellt werden, dass das Immunsystem die Malignität erkennt, und andererseits jegliche Immun-Escape Mechanismen der Tumorzelle verhindert werden.

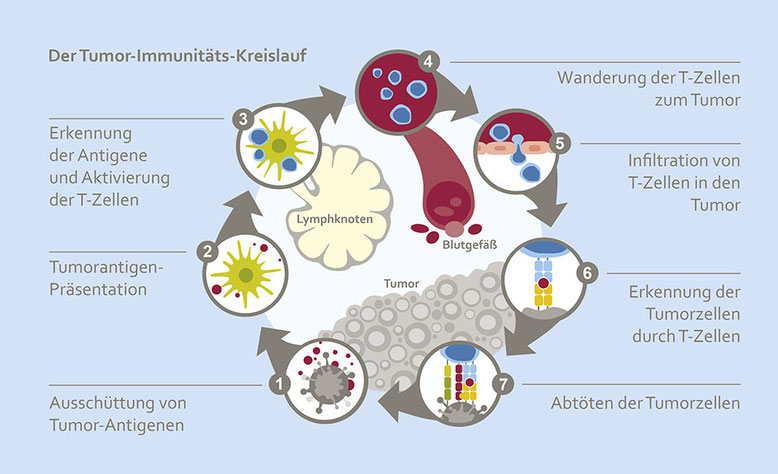
Erkennung von Tumorzellen durch das Immunsystem
T-Lymphozyten können maligne Zellen von gesunden Zellen unterscheiden, wenn diese Neoantigene aufweisen, welche über den MHC von antigenpräsentierenden Zellen, wie dendritischen Zellen, in den regionären Lymphknoten gezeigt werden. Durch den Kontakt mit dendritischen Zellen werden T-Lymphozyten aktiviert, gelangen in die Blutbahn und greifen Tumore mit dem entsprechenden Neoantigen an.
Für eine gelungene Immunantwort muss jeder dieser Schritte stattfinden. An verschiedenen Stellen dieses Ablaufes kann therapeutisch nachgeholfen werden.
Immuntherapie mit Neoantigen-Peptid-Vakzinierung
Neoantigene unterscheiden sich von Antigenen auf gesunden Körperzellen und sind somit der spezifische Ansatzpunkt für eine Tumorvakzinierung. Neoantigene, welche für eine Vakzinierung in Frage kommen, werden nach einem detailliertem Tumor Profiling für jeden Patienten individuell bestimmt.
Dazu ist eine Tumor-Biopsie nötig. Mittels Whole Exome Sequencing werden die gesamten codierenden Regionen der Tumor-DNA analysiert und mit gesunder DNA (aus einer Blutprobe) verglichen. Genveränderungen, welche zu einer veränderten Aminosäuresequenz im Genprodukt führen, sind potentielle Neoantigene.
Aus der Vielzahl der bestimmten Neoantigene werden diejenigen gewählt, welche auch tatsächlich vom Tumor exprimiert werden. Die Expressionsrate wird mit Next Generation Sequencing der Tumor RNA ermittelt. Desweiteren wird die Immunogenitätsrate und die Self-Similarity der ermittelten Neoantigene sowie ihre Bindungsstärke zu HLA-Komplexen berechnet. Für die Vakzinierung werden die Neoantigen-Peptide mit den besten Scores ausgewählt und synthetisch hergestellt.
Wirkung und Nebenwirkung der Krebsimpfung
Die Vakzinierung mit Neoantigenen zur Behandlung von Tumorerkrankungen ist eine neue Methode, welche laut erster Studien sehr vielversprechend ist. Da die T-Lymphozyten spezifisch auf die Neoantigene des patienteneigenen Tumors aktiviert werden, ist eine gezielte Wirkung mit wenig bis keinen Nebenwirkungen zu erwarten.
Weitere Studienergebnisse sind abzuwarten um genaue Aussagen über Wirkung und Nebenwirkungen zu machen. Die Methode befindet sich derzeit in klinischer Untersuchung. Die Krebsimpfung mit Neoantigenen kann daher nicht eine vollständige Krebstherapie ersetzen und stellt einen individuellen Heilversuch dar.

Die Balance des Immunsystems
Die Vakzinierung mit Neoantigenen zur Behandlung von Tumorerkrankungen ist eine neue Methode, welche laut erster Studien sehr vielversprechend ist. Da die T-Lymphozyten spezifisch auf die Neoantigene des patienteneigenen Tumors aktiviert werden, ist eine gezielte Wirkung mit wenig bis keinen Nebenwirkungen zu erwarten.
Weitere Studienergebnisse sind abzuwarten um genaue Aussagen über Wirkung und Nebenwirkungen zu machen. Die Methode befindet sich derzeit in klinischer Untersuchung.
Die Krebsimpfung mit Neoantigenen kann daher nicht eine vollständige Krebstherapie ersetzen und stellt einen individuellen Heilversuch dar.
Checkpoints – die Kontrollpunkte des Immunsystems
Immun-Checkpoints sollen genau diese Balance einhalten, sie kontrollieren die Notwendigkeit des Eingreifens des Immunsystems. Dieser Mechanismus wird von Tumorzellen als Immun-Escape genutzt, indem sie Checkpoints auf der Oberfläche präsentieren, welche dem Immunsystem ein Signal zum Nicht-Angreifen übermitteln.
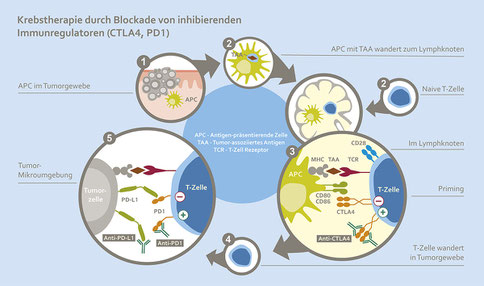
Checkpoint-Inhibitoren – Die Bremse des Immunsystems lösen
In Fällen, wo Checkpoints das Angreifen von Immunzellen auf den Tumor verhindern, kann eine Immuntherapie mit einem Checkpoint-Inhibitor sinnvoll sein. Checkpoint-Inhibitoren, sind Antikörper welche entweder an den Checkpoint (Nivolumab oder Pembrolizumab auf PD-1) oder auf dessen Liganden (Atezolizumab auf PD-L1) binden, somit die Interaktion (z.B.: PD1-PD-L1) verhindern und die Wirkung des Checkpoints aufheben.
Eine körpereigene antitumorale Immunantwort kann dann stattfinden, wenn tumorspezifische zytotoxische T-Zellen vorhanden sind.
Wirkung und Nebenwirkungen der Checkpoint-Inhibitoren
Checkpoint-Inhibitoren können also durch die Unterbrechung der „Nicht-Angriffs-Signalübertragung“ dazu führen, dass das körpereigene Immunsystem erfolgreich gegen den Krebs arbeitet. In vielen Fällen hat dies zu herausragenden Behandlungserfolgen geführt.
Damit die Wirkung allerdings auch zustande kommt, müssen die Lymphozyten zunächst auch spezifisch den Krebs erkennen und tatsächlich am Krebs ankommen. Beides ist nicht immer der Fall und dann ist die Wirkung der Checkpoint-Inhibitoren eingeschränkt.
Es gibt die Möglichkeit, den Status des Immunsystems im Blut und anhand einer Biopsie auch im Tumor festzustellen.
Checkpoint-Inhibitoren können, da sie das Immunsystem enthemmen, auch dazu führen, dass gesunde körpereigene Zellen vom Immunsystem angegriffen werden. Dann können Autoimmunreaktionen entstehen. Zu diesen Nebenwirkungen gehören unter anderem Hautreaktionen, Lungenentzündung oder Dickdarmentzündung welche einen Therapieabbruch nötig machen können.
Diagnostik – Wissen wo es hakt im Immunsystem
Wie für eine gelungene Krebsbehandlung eine intensive Diagnostik immer nötig ist, sollte eine Immuntherapie auch mit entsprechender Feststellung des Immunstatus verbunden sein. In einer Blutprobe können die verschiedenen Immunzellen und Immunsignalstoffe (Zytokine) untersucht werden.

Auch der Immunstatus direkt im Tumor kann wichtig sein bei einer Therapieentscheidung. An einer Biopsie wird der Anteil zytotoxischer und regulativer T-Lymphozyten, tumorassoziierter Makrophagen und die Exprimierung von Checkpoints bestimmt.